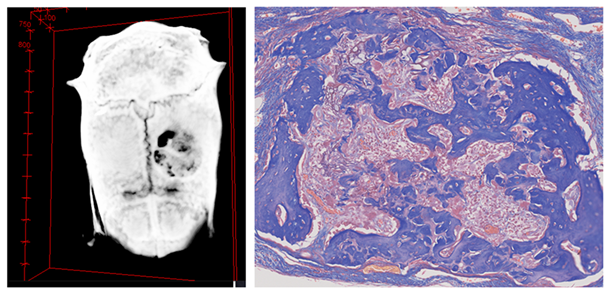
我々は、東京大学古月研究室との共同研究により、リン酸カルシウムを約100 nm 程度まで粉砕・微粒子化し、コラーゲン足場材料(スキャフォールド)に配合することで、材料の生体活性(バイオアクティビティ)を向上させることに成功しました。得られたリン酸カルシウムナノ微粒子は吸収性に優れ、タンパク質吸着やマクロファージの集積を促進することが確認されており、歯周組織再生を目的としたバイオマテリアルとして優れた特性を有すると考えられます。さらに、下図に示すように、β-トリカルシウムリン酸(β-TCP)ナノ微粒子を配合したコラーゲン足場材料は、ラット頭蓋骨モデルにおいて骨再生を誘導しました。本研究は2013年の Journal of Nanomaterialsに掲載されました。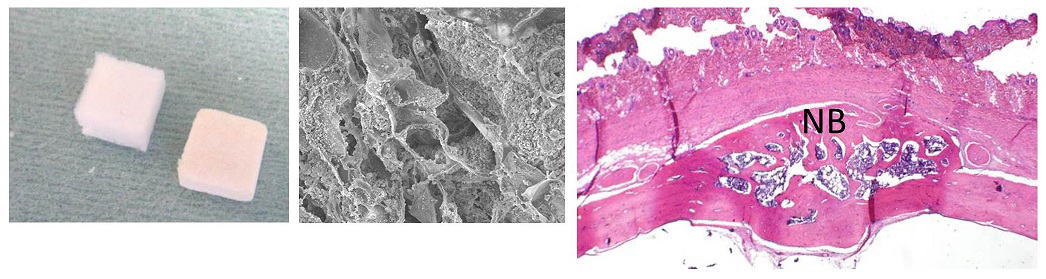
β-トリカルシウムリン酸(β-TCP)単独で高気孔性の足場材を作製した場合、機械的強度が不足するため、生体プラスチックであるポリ乳酸‐グリコール酸共重合体(PLGA)による補強を行ったスキャフォールドを作製しました。歯周組織再生薬リグロスの主成分である線維芽細胞増殖因子(FGF)を添加して再生実験を行った結果、スキャフォールドは生体内で圧縮されることなく再生の場を維持し、十分な骨増生が認められました。本研究は2015年のJournal of Periodontal Researchに掲載されました。
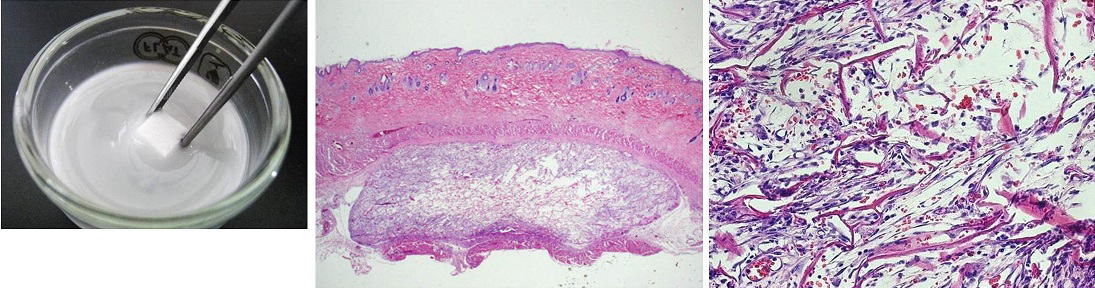
β-トリカルシウムリン酸(β-TCP)ナノ微粒子を配合したスキャフォールドをラットの皮下組織へ埋植する実験を行いました。その結果、細胞や血管が早期から大量にコラーゲン内部へ侵入している様子(イングロース)が観察されました。これらの所見から、ナノ微粒子の添加により、コラーゲン足場材料の多様な生体活性が向上することが明らかとなりました。本研究は2017年のDental Materials Journalに掲載されました。
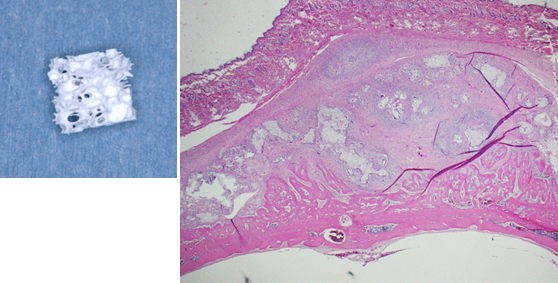
β-トリカルシウムリン酸(β-TCP)ナノ微粒子を配合したスキャフォールドを用いて、イヌ実験的歯周炎モデル(1壁性欠損)における歯周組織再生実験を行いました。その結果、下図に示すように、本スキャフォールドが歯周組織再生を促進することが明らかとなりました。さらに、歯周組織再生薬リグロスの主成分である線維芽細胞増殖因子(FGF2)を併用した場合には、歯周組織の再生量が大幅に増加することが確認されました。本研究は2016年のJournal of Periodontal Researchに掲載されました。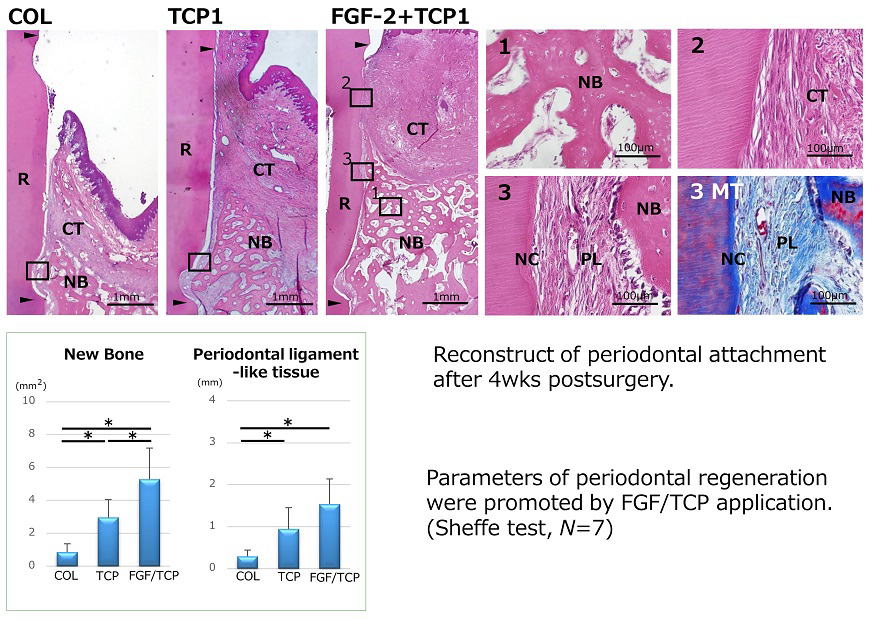
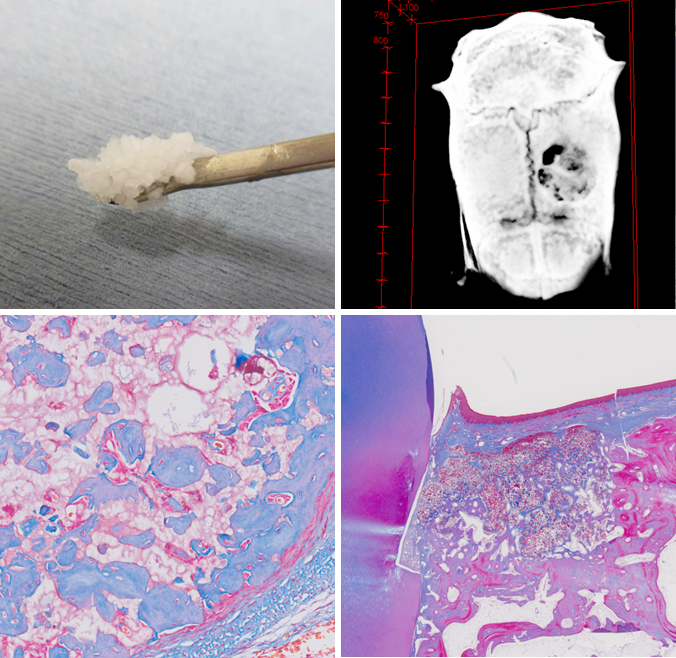
リコンビナントヒトコラーゲン様ペプチド(RCP)は、遺伝子工学的手法により産生された、動物由来成分を含まないバイオマテリアルであり、高い安全性と信頼性を有しています(富士フイルムHP)。我々は、リコンビナントヒトコラーゲン様ペプチド(RCP)を用いて顆粒状の骨補填材を作製し、さらにβ-トリカルシウムリン酸(β-TCP)ナノ微粒子を配合した材料を開発しました。本材料を用いて、ラット頭蓋骨欠損モデルへの埋植実験を行った結果、RCP–β-TCP 複合体は極めて高い骨形成能を示しました。さらに、イヌ歯周組織欠損モデルに埋植したところ、歯槽骨の再生に加えて歯根膜の形成も認められ、歯周組織再生材料として高いポテンシャルを有することが確認されました。本研究は2020年のJ Biomed Mater Res Part B Appl Biomater、2023年のJ Oral Biosciに掲載されました。
Banerjee K, Oyane A, Nakamura M, Inose T, Nishida E, Shitomi K, Miyaji H. Integration of dual drugs into a collagen scaffold by a combination of apatite coating and impregnation with apatite particles for periodontal regeneration. RSC Adv. 2025 Jun 9;15(24):19480-19488.
https://doi.org/10.1039/d5ra02963e
Pal A, Oyane A, Nakamura M, Koga K, Nishida E, Miyaji H. Fluoride-Incorporated Apatite Coating on Collagen Sponge as a Carrier for Basic Fibroblast Growth Factor. Int J Mol Sci. 2024 Jan 25;25(3):1495.
https://doi.org/10.3390/ma17092035
Fujino S, Hamano S, Tomokiyo A, Sugiura R, Yamashita D, Hasegawa D, Sugii H, Fujii S, Itoyama T, Miyaji H, Maeda H. Dopamine is involved in reparative dentin formation through odontoblastic differentiation of dental pulp stem cells. Sci Rep. 2023 Apr 6;13(1):5668.
https://doi.org/10.1038/s41598-023-32126-1
Yoshino Y, Miyaji H*, Nishida E, Kanemoto Y, Hamamoto A, Kato A, Sugaya T, Akasaka T. Periodontal tissue regeneration by recombinant human collagen peptide granules applied with β-tricalcium phosphate fine particles. J Oral Biosci. 2023 Mar;65(1):62-71.
https://doi.org/10.1016/j.job.2023.01.002
Y Kanemoto, H Miyaji*, E Nishida, S Miyata, K Mayumi, Y Yoshino, A Kato, T Sugaya, T Akasaka, AJ Nathanael, S Santhakumar, A Oyane*. Periodontal tissue engineering using an apatite/collagen scaffold obtained by a plasma- and precursor-assisted biomimetic process. J Periodont Res, 57(1), 205-218, 2022.
https://doi.org/10.1111/jre.12954
S Santhakumar*, A Oyane*, M Nakamura, Y Yoshino, MK Alruwaili, H Miyaji*. Bone tissue regeneration by collagen scaffolds with different calcium phosphate coatings: amorphous calcium phosphate and low-crystalline apatite. Materials, 14(19), 5860, 2021.
https://doi.org/10.3390/ma14195860
S Santhakumar*, A Oyane*, M Nakamura, K Koga, S Miyata, K Muratsubaki, H Miyaji. In situ precipitation of amorphous calcium phosphate nanoparticles within 3D porous collagen sponges for bone tissue engineering. Mater Sci Eng C, 116, 111194, 2020.
https://doi.org/10.1016/j.msec.2020.111194
T Furihata, H Miyaji*, E Nishida, A Kato, S Miyata, K Shitomi, K Mayumi, Y Kanemoto, T Sugaya, T Akasaka. Bone forming ability of recombinant human collagen-peptide granules applied with β-tricalcium phosphate fine particles. J Biomed Mater Res Part B Appl Biomater, 108 (7), 3033-3044, 2020.
https://doi.org/10.1002/jbm.b.34632
S Murakami, H Miyaji, E Nishida, K Kawamoto, S Miyata, H Takita, T Akasaka, B Fugetsu, T Iwanaga, H Hongo, N Amizuka, T Sugaya, M Kawanami. Dose effects of beta-tricalcium phosphate nanoparticles on biocompatibility and bone conductive ability of three-dimensional collagen scaffolds. Dent Mater J, 36, 573-583, 2017.
http://doi.org/10.4012/dmj.2016-295
AJ Nathanael, A Oyane, M Nakamura, I Sakamaki, E Nishida, Y Kanemoto, H Miyaji. In vitro and in vivo analysis of mineralized collagen-based sponges prepared by a plasma- and precursor-assisted biomimetic process. ACS Appl Mater Interfaces, 9(27), 22185-22194, 2017.
DOI: 10.1021/acsami.7b04776
K Ogawa, H Miyaji, A Kato, Y Kosen, T Momose, T Yoshida, E Nishida, S Miyata, S Murakami, H Takita, B Fugetsu, T Sugaya, M Kawanami. Periodontal tissue engineering by nano beta-tricalcium phosphate scaffold and fibroblast growth factor-2 in one-wall infrabony defects of dogs. J Periodont Res, 51, 758-767, 2016.
DOI:10.1111/jre.12352
S Yoshida, N Wada, D Hasegawa, H Miyaji, H Mitarai, A Tomokiyo, S Hamano, H Maeda. Semaphorin 3A Induces Odontoblastic Phenotype in Dental Pulp Stem Cells. J Dent Res, 95,1282-1290, 2016.
doi:10.1177/0022034516653085
加藤昭人,宮治裕史,小川幸佑,百瀬赳人,西田絵利香,村上秀輔,吉田 崇,田中佐織,菅谷 勉,川浪雅光.β-三リン酸カルシウムナノ粒子配合コラーゲンスキャフォールドのイヌ抜歯窩骨形成促進効果.日歯保存誌59,351-358,2016.
http://doi.org/10.11471/shikahozon.59.351
T Yoshida, H Miyaji, K Otani, K Inoue, K Nakane, H Nishimura, A Ibara, A Shimada, K Ogawa, E Nishida, T Sugaya, L Sun, B Fugetsu, M Kawanami. Bone augmentation using a highly porous PLGA/β-TCP scaffold containing fibroblast growth factor-2. J Periodont Res, 50, 265-273, 2015.
https://doi.org/10.1111/jre.12206
A Ibara, H Miyaji, B Fugetsu, E Nishida, H Takita, S Tanaka, T Sugaya, M Kawanami. Osteoconductivity and biodegradability of collagen scaffold coated with nano-β-TCP and fibroblast growth factor 2. J Nanomater, 2013, 639502 (1-11), 2013.
http://dx.doi.org/10.1155/2013/639502